伦理委员会审查流程
时间:
2026.03.17
一、伦理委员会审查范围
本院医学伦理委员会审查范围包括药物临床试验项目、医疗器械临床试验项目、涉及人的临床科研项目(包括临床流行病学研究、利用人的医疗记录和个人信息的研究、利用人的生物标本的研究等)。审查类别包括初始审查、跟踪审查和复审。
二、伦理委员会审查流程
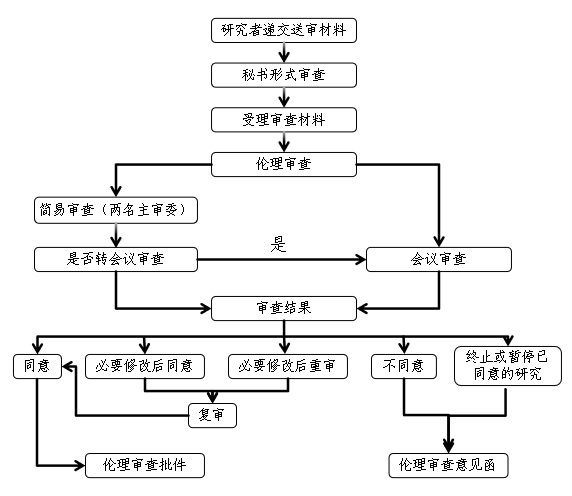
注意事项
1.复审:根据“伦理委员会会议审查意见”,作“作必要修正后同意”或“作必要修正后重审”后,填写“伦理复审申请表”,将修改或补充内容告知伦理委员会,经医学伦理委员会审查同意后方可实施。
2.定期跟踪:依照伦理批件中定期跟踪审查频率要求(在批件有效期前1个月申请递交),研究者应及时提交定期跟踪审查相关材料。

